Ток в електролити
Ток в електролити

електролит
Течен проводник
,
в който
подвижни
носители на заряд
са
само йони

Майкъл Фарадей
Формулирал
законите за
електролизата

Сванте Август Арениус
Шведски химик,
създал през 1884 –
1886 теорията на
електролитната
дисоциация
носител на
химия през
г.

ЕЛЕКТРОЛИТНА
ДИСОЦИАЦИЯ
Разпадането
на молекулите
на йони
под действието на
-
разтворител
или
-
силно нагряване
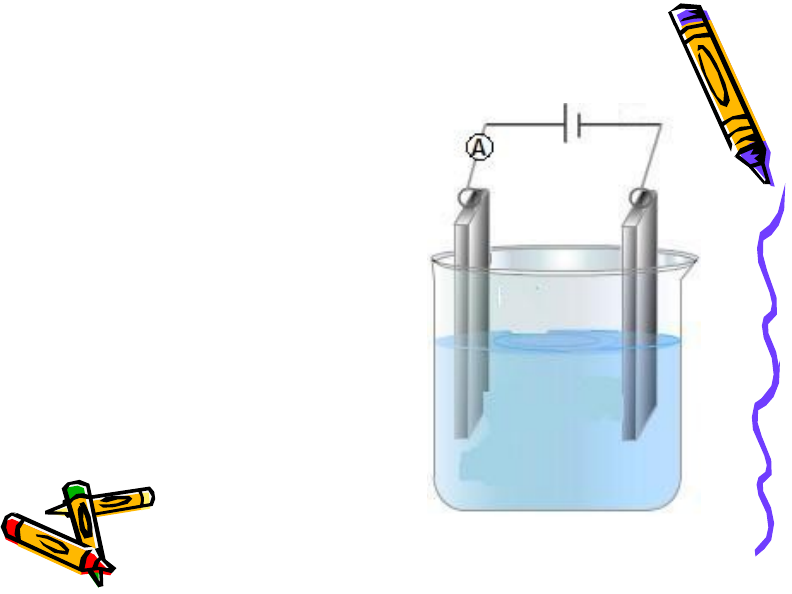
опит
• Свързваме
показаната верига
и наливаме във
ваната
дестилирана вода
• Ток НЕ тече
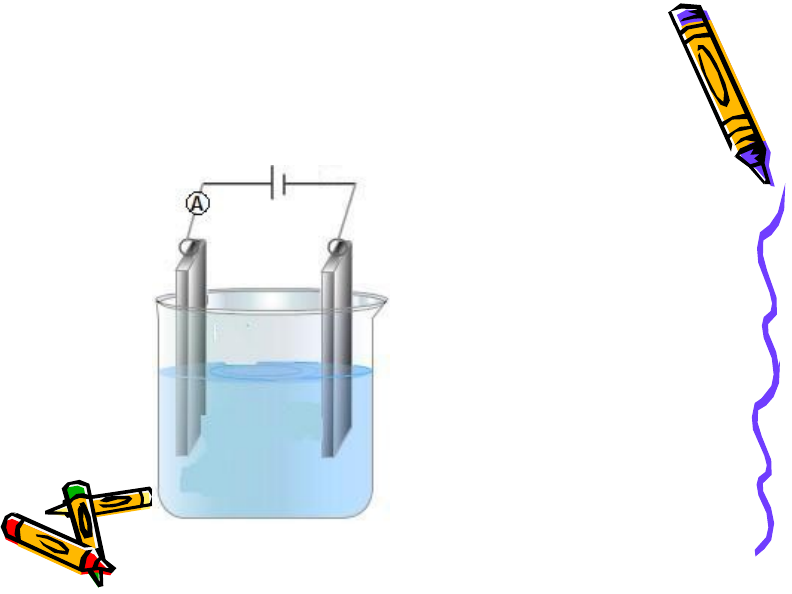
опит
• Добавяме към
дестилираната
вода захар
• Ток Не тече

опит
• Добавяме към
дестилираната вода
готварска сол
• По веригата протича
ток
• Колкото повече сол
добавяме, толкова
по- силен е токът

Опитът илюстрира факта, че
Във воден разтвор ( или стопилка)
молекулите на някои вещества
(например киселини, основи и
соли) се разпадат на
положителни
и
отрицателни
йони
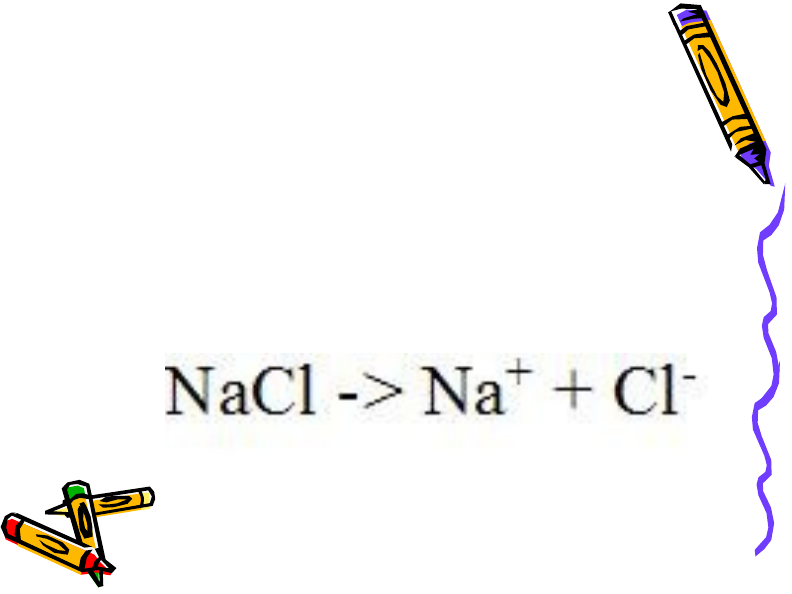
Процесът на
разпадане
се нарича
Електролитна дисоциация

Рекомбинация
–
при среща
два противоположно
заредени йона
могат да
образуват молекула
• Противоположният процес на дисоциацията
• Протича едновременно с дисоциацията
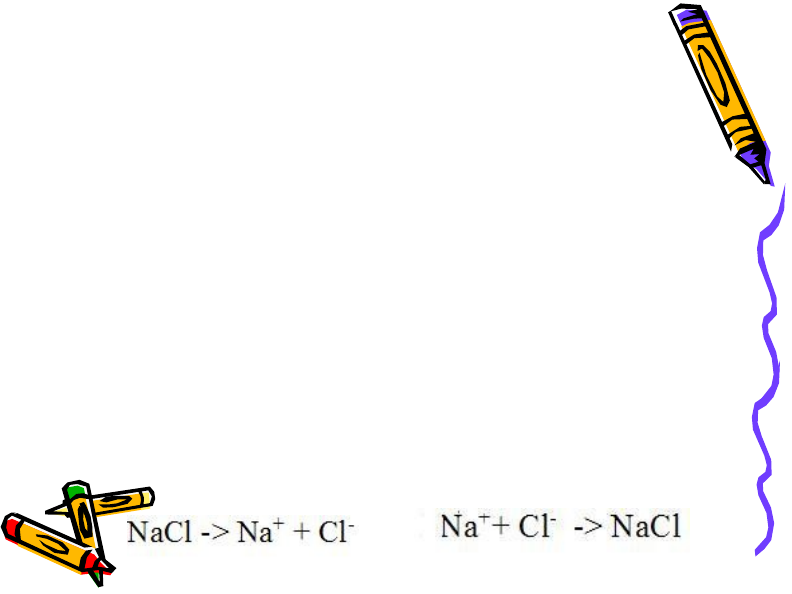
При всяка температура
между
дисоциацията
и
рекомбинацията
настъпва
динамично равновесие
Броят на молекулите,
които се разпадат за =
единица време
Броят на
рекомбиниралите за
единица време
двойки йони

В разтвора се установява
определена концентрация на йони

Концентрацията на йоните
зависи от:
• Концентрацията на разтвора
• Температурата
• Вида на разтворителя
Какво е животът?
Есе по произведението на Георги Господинов "Кристин, която маха от влака" на тема "Намесата в чуждия живот"...Какво е животът?
| Предмет: | Литература |
| Тип: | Есета |
| Брой страници: | 2 |
| Брой думи: | 606 |
| Брой символи: | 3262 |